I biocatalizzatori basati su enzimi immobilizzati hanno ricevuto notevole attenzione grazie a importanti applicazioni nella sintesi di prodotti chimici, prodotti farmaceutici e intermedi farmaceutici a valore aggiunto con grande efficienza catalitica ed elevate rese di molecole bersaglio. Gli importanti vantaggi di tali biocatalizzatori sono una maggiore stabilità in un intervallo di pH e temperatura, la separazione dalle soluzioni di reazione, la stabilità nell’uso ripetuto.
I biocatalizzatori, detti anche catalizzatori intelligenti presentano, rispetto ai catalizzatori tradizionali, una elevata specificità, condizioni di reazione più blande e velocità di reazione più rapide. Tra i vantaggi offerti dai biocatalizzatori vi è l’elevata selettività nella produzione di singoli stereoisomeri, l’esclusione di reazioni secondarie, la diminuzione di operazioni di ritrattamento e purificazione e la sostenibilità del processo.
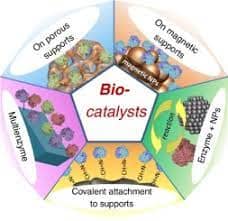
I biocatalizzatori, infatti, hanno mostrato un’elevata selettività e specificità nei confronti del loro substrato in condizioni blande rispetto a processi chimici che vengono eseguiti in condizioni molto difficili e portano a sottoprodotti collaterali indesiderati. Inoltre la natura biologica degli enzimi li rende meno pericolosi per la salute e meno tossici per l’ambiente rispetto ai catalizzatori chimici.
Uno dei primi esempi di biocatalizzatori furono i microrganismi come la muffa Penicillium glaucum in qualità di enzimi utilizzati da Louis Pasteur nel 1858 in una reazione di fermentazione al fine di produrre acido tartarico. Oggi i biocatalizzatori, unitamente ai liquidi ionici, costituiscono un supporto indispensabile per nuove tecnologie sostenibili. Pertanto la selezione di enzimi con alta affinità verso il substrato, alto numero di turnover ed efficienza catalitica da usare come biocatalizzatori è necessaria per applicazioni industriali di successo.
Biocatalizzatori e nuove sfide
Nonostante tutti i progressi fatti negli ultimi anni i biocatalizzatori presentano alcune problematiche che costituiscono una sfida per le applicazioni tecnologiche. Innanzi tutti l’elevato costo di enzimi puri, la bassa velocità delle reazioni catalizzate da enzimi e la loro scarsa resistenza in metodologie prive di solventi. L’uso mirato di tensioattivi, additivi e diverse strategie sposterebbe il campo a nuovi e più efficienti livelli.
Il problema della perdita di enzimi dovuta all’instabilità dei biocatalizzatori deve essere ridotto al minimo con opportune ricerche sull’inibizione, la frammentazione meccanica dovuta all’agitazione, la lisciviazione dell’enzima dal biocatalizzatore nel mezzo di reazione, la fase di separazione o il pretrattamento prima di ulteriori utilizzi, la purificazione del prodotto a valle e il ricircolo dell’enzima immobilizzato.
I costi reali relativi all’immobilizzazione degli enzimi, al riutilizzo, alla lisciviazione e alla perdita di attività durante lo stoccaggio devono essere ottenuti con informazioni, procedure e metodi adeguati. Pertanto vengono sviluppate sempre di più in diversi campi le tecnologie relative a biosensori enzimatici per la medicina, microreattori stampati in 3D per test microfluidici, reattori a membrana, diverse reazioni a cascata e reattori multienzimatici in cascata.
Downstreaming
Le varie fasi o operazioni unitarie eseguite per separare e purificare il prodotto dopo il processo di fermentazione sono definite downstream o elaborazione a valle. Un importante fattore da considerare è il costo della produzione dell’enzima durante la progettazione del processo complessivo.
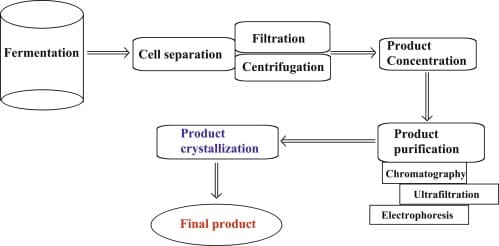
Un altro criterio importante di cui si tiene conto durante l’operazione di downstreaming è la purezza degli enzimi oltre al numero di passaggi che influisce sulle prestazioni complessive e sui costi di produzione di un prodotto. Gli enzimi possono essere prodotti a livello extracellulare o intracellulare e il numero di passaggi è maggiore nel recupero degli enzimi intracellulari e pertanto il costo di produzione degli enzimi intracellulari è maggiore rispetto a quello degli enzimi extracellulari.
Le varie fasi del downstreaming prevedono l’estrazione, la separazione, la concentrazione, la purificazione e infine la formulazione del prodotto desiderato. Il funzionamento di ciascuna unità viene ottimizzato prima di procedere alla fase successiva. Dopo la fermentazione, l’enzima prodotto viene separato dal resto della coltura e dal mezzo tramite determinate tecniche come la filtrazione o la centrifugazione. La maggior parte degli enzimi prodotti sono di natura extracellulare e quindi richiedono metodi di estrazione semplici. Gli enzimi intracellulari richiedono alcune tecniche aggiuntive di distruzione cellulare.
La distruzione delle cellule microbiche può essere meccanica o non meccanica. Dopo il rilascio dell’enzima grezzo, questo è stato concentrato tramite precipitazione di sale o solvente. Il prodotto concentrato viene sottoposto a speciali tecniche di purificazione come cromatografia, ultrafiltrazione ed elettroforesi per ottenere l’enzima altamente purificato.
Degradazione enzimatica della plastica
Gli enzimi sono biocatalizzatori che partecipano a una reazione, agiscono su un particolare substrato e accelerano il processo di conversione di quel substrato in un prodotto prezioso. Molti enzimi sono stati isolati da alghe, attinomiceti, batteri e funghi che sono noti per causare la degradazione in molte forme di materiali plastici
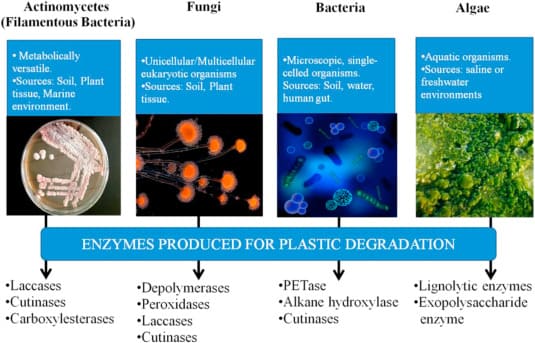
I polimeri sintetici derivanti dal petrolio come polietilene, polietilentereftalato, poliuretani, polistirene, polipropilene e polivinilcloruro sono ancora fondamentali nel nostro stile di vita ma il loro accumulo rappresenta una delle principali preoccupazioni per l’ambiente e la salute umana.
La degradazione della plastica mediante biocatalizzatori è una strategia promettente per depolimerizzare i rifiuti polimerici in monomeri da riciclare, o mineralizzarli in anidride carbonica, acqua e nuova biomassa, con la produzione concomitante di bioprodotti di valore superiore. Negli ultimi 10 anni sono stati compiuti progressi significativi nella comprensione della degradazione enzimatica delle plastiche idrolizzabili. Molti studi scientifici hanno annunciato la scoperta di microrganismi che degradano le materie plastiche e hanno fornito prove dell’esistenza di enzimi responsabili della degradazione della plastica.
Tutti gli enzimi noti per degradare i polimeri plastici appartengono alla classe delle idrolasi e sono coinvolti in una reazione catalitica che provoca la rottura dei legami chimici del suo substrato in presenza di acqua provocando la scissione idrolitica delle lunghe catene di carbonio e quindi assimilando queste subunità più piccole nella cellula microbica per un’ulteriore degradazione enzimatica e il rilascio di prodotti metabolici
I biocatalizzatori presenti in microrganismi, funghi e batteri, possiedono meccanismi di degradazione delle materie plastiche. I biocatalizzatori utilizzano la plastica come unica fonte di carbonio per la loro sopravvivenza e quindi possono utilizzare i polimeri quando vengono fornite le condizioni ottimali necessarie per una loro crescita più rapida.
Questo processo può essere ulteriormente modificato se la plastica viene trattata prima dell’attacco microbico per scomporre il polimero in unità monomeriche attraverso metodi chimici o fisici tra cui riscaldamento, raffreddamento, congelamento, scongelamento e degradazione chimica.
